Un equipo de científicos, liderados por Ryotaro Hashizume, ha logrado eliminar el cromosoma extra responsable del síndrome de Down mediante la técnica de edición genética CRISPR-Cas9. Este avance representa un paso prometedor hacia posibles tratamientos, aunque todavía existen desafíos antes de su aplicación en humanos. La investigación sugiere que, en el futuro, la edición genética podría corregir la trisomía 21 en células cerebrales, restaurando la función normal.
Edición genética para eliminar cromosoma extra
El síndrome de Down es una condición genética causada por la presencia de un tercer cromosoma 21. Afecta a aproximadamente 1 de cada 700 nacimientos y, aunque se puede detectar en etapas tempranas del desarrollo, actualmente no existen tratamientos que modifiquen la base genética de la afección.
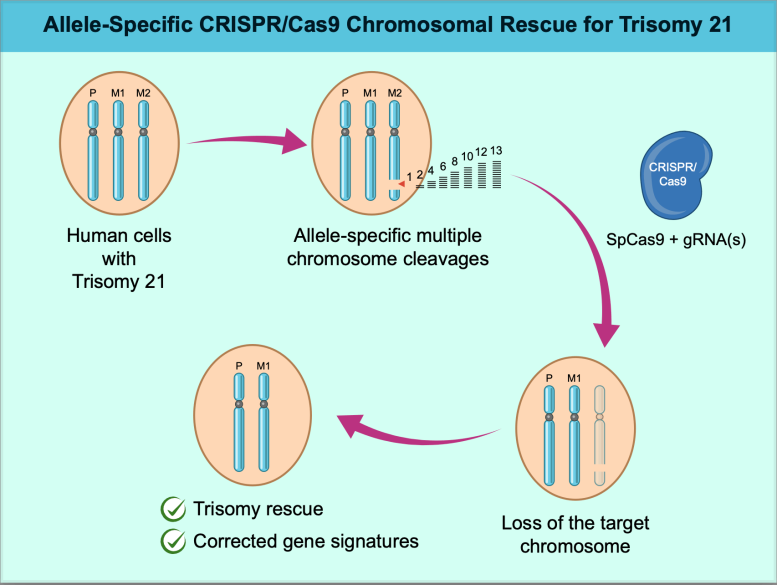
La investigación, liderada por Ryotaro Hashizume y su equipo, utilizó CRISPR-Cas9 para eliminar la copia adicional del cromosoma 21 en células cultivadas en laboratorio. Estas células provenían de fibroblastos de la piel y células madre pluripotentes, lo que permitió a los científicos evaluar la eficacia del método en diferentes tipos celulares.
Uno de los principales retos de esta técnica es garantizar que, tras la eliminación del cromosoma extra, las células mantengan una copia de cada progenitor en lugar de dos copias idénticas. Para lograrlo, los investigadores desarrollaron un enfoque que identifica y ataca exclusivamente al cromosoma duplicado sin afectar el resto del material genético.
Restauración de la expresión génica

La eliminación del cromosoma extra no solo modificó la estructura genética de las células, sino que también tuvo un impacto en su funcionamiento. Al restaurar la expresión génica normal, las células editadas recuperaron su actividad biológica típica, lo que sugiere que la eliminación del cromosoma adicional podría corregir algunos de los efectos de la trisomía.
El estudio también reveló que al suprimir ciertos mecanismos naturales de reparación del ADN, se aumentó la eficiencia del procedimiento. Esto es clave para futuras aplicaciones, ya que permitiría mejorar la precisión de la técnica y reducir el riesgo de alterar cromosomas no deseados.
Si bien el experimento tuvo éxito en células cultivadas en laboratorio, su aplicación en organismos vivos sigue siendo un desafío. Uno de los principales riesgos es la posibilidad de que la edición genética afecte otros cromosomas, generando efectos no deseados.
Sin embargo, los investigadores creen que, con más desarrollo, enfoques similares podrían utilizarse para modificar neuronas y células gliales. Esto abriría la puerta a tratamientos innovadores para el síndrome de Down, especialmente en etapas tempranas del desarrollo, cuando la plasticidad cerebral es mayor.
Además, la edición genética podría combinarse con terapias regenerativas para corregir anomalías celulares y mejorar la calidad de vida de los pacientes. A medida que la tecnología avance, se espera que los tratamientos basados en CRISPR-Cas9 se vuelvan más seguros y específicos.
Consideraciones éticas y futuro de la investigación

El uso de CRISPR en la modificación de embriones humanos sigue siendo un tema controversial. Si bien esta tecnología tiene el potencial de corregir enfermedades genéticas, también plantea cuestiones éticas sobre la manipulación del ADN y los posibles efectos a largo plazo.
Actualmente, la comunidad científica aboga por un enfoque cauteloso y regulado. Antes de que estas técnicas puedan aplicarse en humanos, será necesario realizar estudios adicionales para evaluar su seguridad y eficacia. Los avances en edición genética representan una esperanza para muchas personas, pero también requieren un marco legal y ético que garantice su uso responsable.
La eliminación del cromosoma extra en células con trisomía 21 mediante CRISPR-Cas9 marca un avance significativo en la investigación del síndrome de Down. Aunque aún no es aplicable en humanos, este descubrimiento abre nuevas posibilidades para el desarrollo de terapias genéticas. Con más estudios y refinamientos, la edición genética podría ofrecer en el futuro una solución real para quienes padecen esta condición.
Referencia:
- PNAS/Trisomic rescue via allele-specific multiple chromosome cleavage using CRISPR-Cas9 in trisomy 21 cells. Link.