
Un nuevo tratamiento basado en una terapia de captura de neutrones con boro, se está usando en Japón para atacar directamente y tratar tumores de cabeza y cuello. Muchos de los demás países están construyendo instalaciones para realizar el mismo tratamiento al ver su grado de efectividad.
Tratamiento pionero contra el cáncer
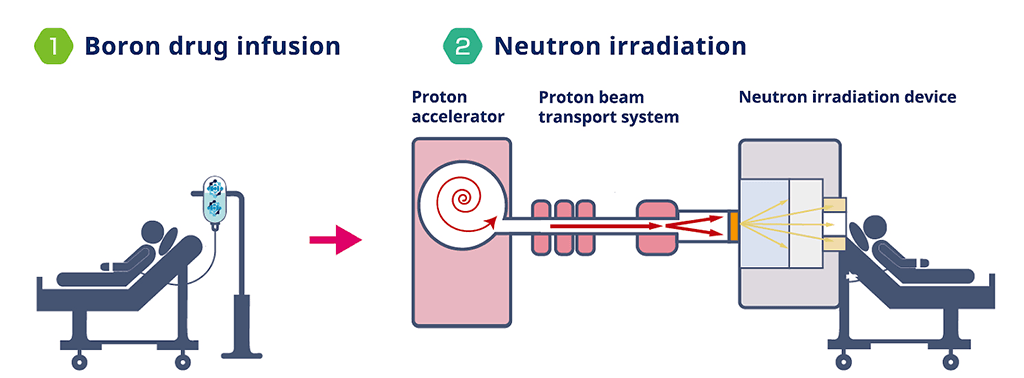
En 2020, Japón fue el primer país en probar la terapia de captura de neutrones con boro, o BNCT, por sus siglas en inglés. Esto se trata de una radioterapia dirigida para pacientes que sufren de cáncer.
Como otras radioterapias, la BNCT envía rayos de radiación al cuerpo para matar las células cancerosas. Pero este nuevo tratamiento usa haces menos intensos, empleando una interacción específica entre el boro en el tumor y los neutrones en el haz, liberando una potente radiación local, lo que disminuye considerablemente el daño al tejido sano.
En Japón, la BNCT se aprobó para tratar tumores en la cabeza y cuello que son irresacables, avanzados y recurrentes, explicó el director del Centro Médico Kansai BNCT de la Universidad Médica y Farmacéutica de Osaka, Koji Ono. Los tratamientos estándar, como la quimioterapia, otras radioterapias o productos farmacéuticos dirigidos, siguen siendo la primera opción para el cáncer de cabeza y cuello. Pero BNCT ya está disponible para casos más complicados.
En Japón, hasta la fecha, más de 500 pacientes han sido tratados con este tratamiento y su número aumenta cada año.
Efecto sorprendente
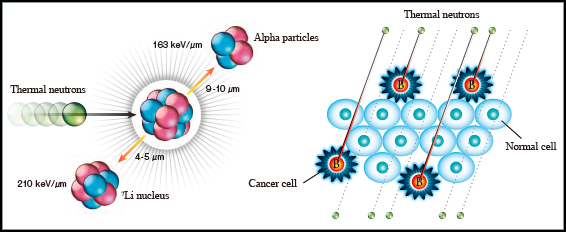
La radioterapia tradicional usa haces de radiación ionizante, como rayos X o iones de carbono. Pero BNCT usa un método que causa menos daño al tejido entre las células tumorales. Para ello, a los pacientes se les administra un fármaco que contiene boro diseñado para acumularse en células tumorales. Después, los médicos usan una corriente de neutrones de baja energía usando un acelerador de partículas compacto, irradiando el tejido tumoral, ahora rico en boro.
Como los neutrones de baja energía no lleven carga eléctrica, no dañan las células por las que pasan. Los efectos anticancerígenos del BNCT surgen de las destructivas partículas alfa y de litio que se producen cuando los neutrones chocan contra un átomo de boro. Entonces, al garantizar que el boro ya esté dentro de las células tumorales, las partículas alfa y de litio que destruyen las células pueden restringirse más fácilmente al tejido tumoral y evitar dañar las células sanas.
La esperanza es que este tratamiento pueda usarse en otros tipos de cánceres, ya que cuando se trata de órganos profundos, es complicado llevar neutrones al lugar del cáncer.
El problema, según Ono, es que los neutrones usados para la BNCT son una forma de radiación relativamente débil y no puede aplicarse profundamente en el cuerpo a niveles terapéuticos. Los cánceres de cabeza y cuello se ubican cerca de la superficie, por ello, son más accesibles.
Mayor concentración
Una posibilidad de tratar tumores profundos es administrar una mayor concentración de boro a los tejidos cancerosos. Así, incluso un débil haz de neutrones puede tener efecto. Los fármacos existentes pueden hacer que el boro se acumule preferentemente en las células tumorales, en comparación con las células normales, en una proporción de aproximadamente 3,5 a 1,0.
El investigador Koki Uehara, presidente y director de operaciones de Stella Pharma Corp en Osaka, está intentando fabricar medicamentos que puedan aumentar la absorción de boro por las células cancerosas Él sabe todo sobre los agentes portadores de boro, ya que Stella produce el único aprobado en Japón para el tratamiento.
Aun hacen falta muchas hazañas de ingeniería para crear este agente. El boro natural viene como una mezcla de dos tipos, pero sólo uno de estos isótopos, el boro 10, absorbe neutrones. Alrededor del 80% del boro natural es boro 11. Stella Chemifa Corp, socio de Stella Pharma, es la única empresa japonesa que tiene una forma de enriquecer el contenido de boro 10 de sus agentes a niveles aceptables para el tratamiento con BNCT en Japón.
Además, Stella Pharma Corp creó una estructura para un agente que se parece mucho a la fenilalina, un metabolito celular básico. Como las células tumorales necesitan fenilalina en grandes cantidades por su rápido crecimiento, esto garantiza una absorción preferencial por parte de las células cancerosas en comparación.
Pero los fármacos que contienen boro son poco solubles en agua, lo que dificulta su introducción al torrente sanguíneo en grandes cantidades. Para que la terapia de neutrones destruya las células cancerosas, los tumores deben acumular más de 20 partes por millón de boro, por lo que los pacientes necesitan dosis intravenosa alta de aproximadamente 500 mg por kilogramo de peso corporal o 30 g del medicamento para una persona de 60 kg.
Sin embargo, el fármaco tiene una solubilidad en agua de solo 0,6 g/litro, lo que significa que el paciente tendría que recibir más de 50 litros de solución por goteo. Para solucionar esto, Uehara dice que la compañía experimentó con aditivos y, finalmente, encontró una mezcla que hizo que su agente fuese casi 100 veces más soluble. Este es el avance que hizo posible la aplicación clínica de BNCT, afirmó.
Otra avance importante para el tratamiento, es la forma en la que se producen los neutrones, aseguró Hiroshi Igaki, jefe del Departamento de Oncología y Radioterápica del Hospital del Centro Nacional del Cáncer de Tokio. La teoría de que el BNCT podría usarse para tratar células cancerosas se planteó por primera vez en 1936, apenas cuatro años después de que se descubrieran los neutrones. Pero durante décadas, la única fuente viable de neutrones era un reactor nuclear.
Eso cambió con el desarrollo de un sistema BNCT compacto basado en un acelerador. Los aceleradores usan campos electromagnéticos o campos eléctricos de radiofrecuencia para impulsar partículas cargadas a velocidades y energías altas. Al ajustar la energía de aceleración de su sistema, este proceso ahora se puede usar para producir un suministro estable de neutrones.
Tecnología compacta

En Japón, el sistema BNCT basado en acelerador desarrollado por Sumitomo Heavy Industries Ltd. Recibió la aprobación regulatoria en 2020. Otros dispositivos similares desarrollados por CICS Inc. están siendo sometidos a ensayos clínicos en el Hospital del Centro Nacional del Cáncer. Pero aunque sigue siendo compleja y costosa, dicha tecnología ofrece una fuente de neutrones más conveniente.
Al ver los resultados, otros países han comenzado a trabajar en el mismo tratamiento. Según la Agencia Internacional de Energía Atómica, actualmente hay 33 instalaciones del BNCT disponibles o en construcción, en países desde el Reino Unido hasta Tailandia.
Los investigadores en Japón también han explorado si el tratamiento ayudaría a tratar otros tipos de cáncer. Igaki sigue investigando su uso para tratar una variedad de cánceres, incluyendo un estudio de pacientes con angiosarcomas del cuero cabelludo, que son cánceres de los vasos sanguíneos y linfáticos. Aseguró que los resultados le dan esperanza de un uso más amplio.
Esta podría ser una luz de esperanza. Una puerta que se abre en la búsqueda de encontrar una cura que no sea tan agresiva a una enfermedad tan degenerativa como el cáncer. De momento, solo queda esperar y ver cómo transcurre su avance. El estudio científico puede leerse aquí.
